专为高中生提供有价值的资讯
金属活动性顺序是历年来中考命题的热点,题目的难易不同,题型各异。因此对金属活动性顺序表的正确理解和灵活运用十分重要。
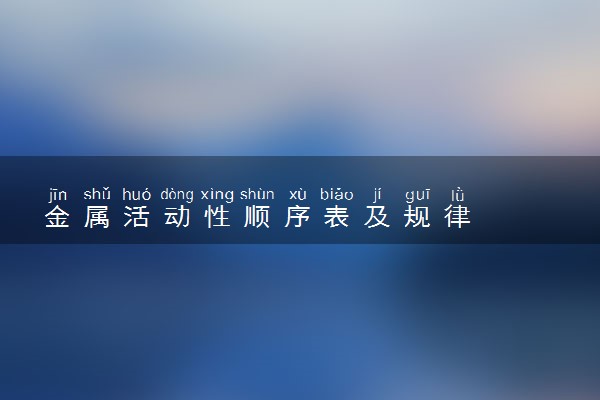
K Ba Ca Na Mg Al Mn Zn Cr Fe Co Ni Sn (H) Cu Hg Pb Ag Pt Au
即:钾钡钙钠镁铝锰锌铬铁钴锡铅氢铜汞银铂金
各种金属的金属性从左到右递减,对应金属的简单的,一般正价的离子氧化性从左到右递增(特殊:Hg2+<Fe3+<Ag+). 还有Cu(+1);Mn有+2;+4;+7价
金属大概是这样:由强到弱 铯最强 然后是稀土、钡、铷、再然后是钾〉钙〉钠〉镁〉锂〉铝〉铍〉锰〉锌〉铁〉钴〉镍〉锡〉铅〉铜〉汞〉银〉铂〉金。
金属活动性和反应的剧烈程度无关。大多数人认为铯与水反应会爆炸,而锂与水反应很平和,误以为铯比锂活泼,但这种观点是错误的。金属活动性只和其电极电势有关,和剧烈程度无关。因此,锂是活动性最强的金属。
1.排在前面的金属可以将排在后面的金属从它们的金属溶液中置换出来。(若金属过于活泼,则会直接与水反应,并不会与水中的金属离子反应)。
2.理论上讲,金属活动性表中铁及排在其前的金属均可置换出纯水中的氢。
3.若只考虑氢离子的氧化性,排在氢(H)前的金属才能和非氧化性酸反应,置换出氢。
4.排在越后的金属越容易,也越先从它们的化合物中被置换出来;排在越前的金属越容易,也越先把其他化合物中的金属置换出来。
Copyright 2019-2029 http://www.laigaokao.com 【来高考】 皖ICP备19022700号-4
声明: 本站 所有软件和文章来自互联网 如有异议 请与本站联系 本站为非赢利性网站 不接受任何赞助和广告